润新生物RX108临床试验,RX108注射液治疗复发性胶质母细胞瘤的II期临床试验
试验目的
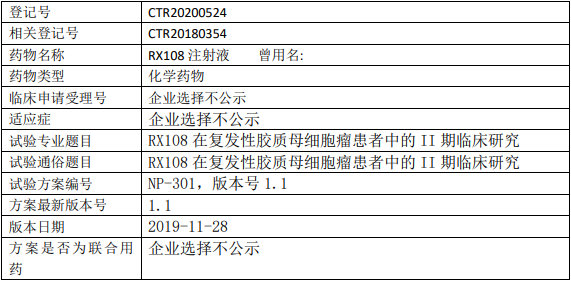
考察RX108在复发性胶质母细胞瘤(rGBM)患者体内的疗效和安全性。
试验设计
试验分类:安全性和有效性
试验分期:II期
设计类型:单臂试验
随机化:非随机化
盲法:开放
试验范围:国内试验
受试者信息
年龄:18岁(最小年龄)至75岁(最大年龄)
性别:男+女
健康受试:者无
出入排标准
入选标准
1、自愿入组并签署知情同意书,遵循试验治疗方案和访视计划。
2、组织学确诊的脑胶质母细胞瘤(GBM),经标准治疗(术后放疗联合替莫唑胺同步和辅助化疗)后出现进展或复发的患者。
3、根据RANO评价标准,患者至少有一处可测量病灶。
4、预期生存期至少3个月。
5、Karnofsky评分≥60。
6、简易精神状态检查量表(MMSE)评分≥15。
7、患者在筛选时满足实验室检查要求。
8、患者如接受过化疗、放疗、生物治疗、内分泌治疗、靶向治疗、免疫治疗等抗肿瘤治疗,则洗脱期至少为4周。
9、患者必须从之前的治疗毒性中恢复至≤1级,脱发和2级既往含铂治疗相关神经病变(CTC AE 5.0),以及研究者认为无安全风险的毒性除外。
排除标准
1、在首次使用研究药物前4周内接受过主要脏器外科手术(不包括穿刺活检)。
2、过去5年内有其他恶性肿瘤病史的患者。
3、接受激素治疗的受试者进入试验前5天内无法接受稳定或剂量降低的类固醇激素治疗。
4、患者存在未被控制的疾病。
5、有免疫缺陷病史,包括HIV抗体检测阳性。
6、活动性乙型肝炎,丙型肝炎病毒感染及活动性梅毒者。
7、妊娠期或哺乳期女性。
8、研究者认为不适合参与本研究。