普锐特药业布地奈德福莫特罗临床试验,评价布地奈德福莫特罗吸入气雾剂治疗哮喘有效性和安全性的III期临床试验
布地奈德福莫特罗临床试验简介
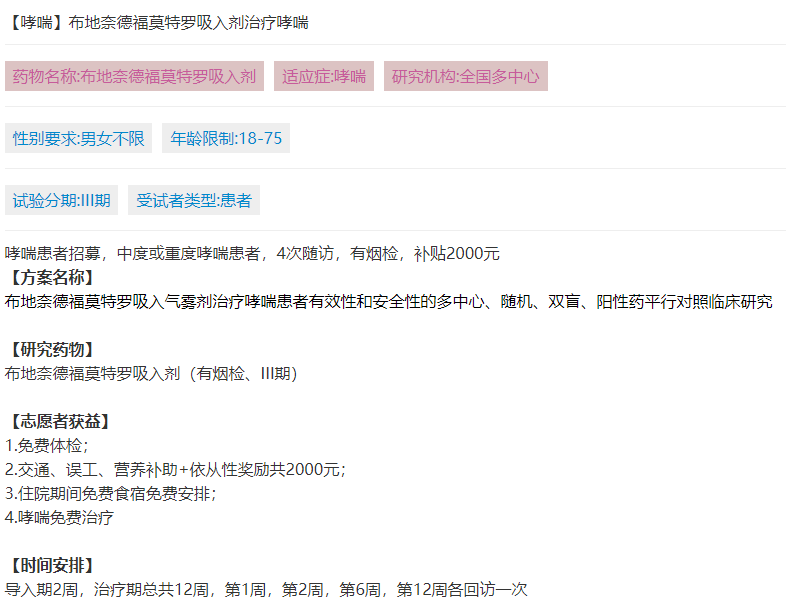
哮喘患者招募,中度或重度哮喘患者,4次随访,有烟检,补贴2000元
【方案名称】
布地奈德福莫特罗吸入气雾剂治疗哮喘患者有效性和安全性的多中心、随机、双盲、阳性药平行对照临床研究
【研究药物】
布地奈德福莫特罗吸入剂(有烟检、III期)
【志愿者获益】
1.免费体检;
2.交通、误工、营养补助+依从性奖励共2000元;
3.住院期间免费食宿免费安排;
4.哮喘免费治疗
【时间安排】
导入期2周,治疗期总共12周,第1周,第2周,第6周,第12周各回访一次
出入排标准
【入选标准】
受试者必须同时满足以下所有选项:
1、年龄18~75周岁(包括边界值),性别不限;
2、根据《2020GINA全球哮喘处理和预防策略》,筛选访视前至少6个月诊断为哮喘(提供可溯源的诊断证明等医疗记录);
3、筛选访视及随机访视,支气管扩张剂使用前的FEV1占预测值>45%且<85%;且满足下列任意一个条件:
①筛选访视时提供既往任何一项可变气流受限的客观检查阳性结果;
②若筛选访视时未能提供既往可变气流受限的客观检查阳性结果,则受试者应当在筛选访视或随机访视前进行支气管舒张试验,且检测结果为阳性(支气管舒张试验阳性定义为吸入支气管舒张剂后FEV1增加>12%且FEV1绝对值增加>200mL);
4、进行肺功能测试时,若使用短效2受体激动剂(SABA)至少间隔6小时,若使用长效受体激动剂(LABA)至少间隔24小时;
5、哮喘严重程度分级为中度或重度;且筛选访视前对于当前的哮喘治疗已经维持稳定至少4周;
6、筛选访视前按需使用SABA或者其他缓解症状类药物的受试者,研究者评估后认为能够使用本研究统一提供的急救药物(硫酸沙丁胺醇吸入气雾剂)替代的方可入组;
7、目前戒烟至少1年,且吸烟史<10包-年[吸烟指数(包年)=每日吸烟量(包)X吸烟时间(年),1包=20支];
8、受试者能够理解本研究的程序和方法,愿意严格遵守临床研究方案完成本研究,并签署知情同意书;
9、受试者接受培训后能够正确使用气雾剂、峰流速仪、填写日记卡。
【排除标准】
凡是出现下列情况之一者不能入选本试验:
1、已知或疑似对任何2受体激动剂,任何糖皮质激素,试验用药品及其他赋形剂过敏者;
2、危及生命的哮喘,定义为筛选访视前1年或导入期内出现需要气管插管的哮喘发作,和/或伴有高碳酸血症、呼吸骤停或低氧惊厥、哮喘相关的晕厥发作、因重度哮喘导致住院;
3、经研究者判断为慢性阻塞性肺疾病(COPD);
4、除哮喘外的其他呼吸系统疾病,如间质性肺病、肺癌、活动性或非活动性肺结核感染、慢性鼻窦炎等,经研究者判断可能会使受试者处于不适当风险或影响研究结果的判断,或筛选访视前4周或导入期出现下呼吸道感染(包括肺炎);
5、严重的心血管疾病,如不稳定性缺血性冠心病、心功能分级Ⅱ-Ⅳ级、心律失常(如室上性心动过速、房颤、频发室早、II-III度房室传导阻滞等)、QTc>480ms、心动过缓(心率或脉搏<50次>160mmHg,或舒张压>100mmHg)等;
6、控制不佳的糖尿病(筛选访视空腹血糖11.1mmol/L);
7、甲状腺功能亢进症;
8、未愈的口腔疾病,如口腔溃疡、口腔黏膜破损、口咽部念珠菌病等;
9、既往患有或正在接受治疗的青光眼、白内障、眼部单纯疱疹的受试者;
10、肝肾功能:
a)肝功能:丙氨酸氨基转移酶(ALT)>2倍正常值上限且天门冬氨酸氨基转移酶(AST)>2倍正常值上限,或碱性磷酸酶(ALP)>1.5倍正常值上限且总胆红素(TBIL)>1.5倍正常值上限;
b)肾功能:肌酐(CRE)>1.5倍正常值上限且肌酐清除率(CrCl)或肾小球滤过率(GFR)60mL/min(Cockcroft-Gault公式);
11、筛选访视血钾3.5mmol/L;
12、筛选访视前4周内口服或注射过糖皮质激素,或筛选访视前6个月内使用过生物靶向药(如奥马珠单抗等),或正在使用细胞色素酶P4503A4抑制剂(如利托那韦、克拉霉素、酮康唑、伊曲康唑等)、受体阻滞剂(包括滴眼剂)、单胺氧化酶抑制剂、三环类抗抑郁药、非保钾利尿剂(如袢利尿剂、噻嗪利尿剂等)的受试者;
13、筛选访视前1年内有吸毒史、药物滥用史或有长期酗酒史(定义为男性每天饮用超过60g的纯酒精(烈酒(40°)约200mL,啤酒约1500mL,红酒约650mL),女性每天饮用超过40g纯酒精(烈酒(40°)约140mL,啤酒约1000mL,红酒约440mL));
14、妊娠或哺乳期妇女或血妊娠检查结果阳性受试者,以及在整个试验期间及研究结束后3个月内有妊娠计划的男性受试者(或其伴侣)或女性受试者;
15、筛选访视前3年内接受过支气管热成形术,或计划在筛选期、导入期或治疗期开始此治疗的受试者;
16、筛选访视前3个月内参加过其它临床试验且使用了试验药物或医疗器械的受试者;
17、根据研究者判定,受试者因身体状况、地理位置或配合程度等原因,而可能对方案任何方面(如访视计划、日记卡填写、峰流速仪使用、肺功能检查或问卷完成等)的依从性产生影响;
18、受试者存在其他有显著临床意义的疾病或者异常、未控制的情况,经研究者判断可能会使受试者处于不适当风险或影响研究结果的判断;
19、研究者认为存在任何可能影响受试者提供知情同意或遵循试验方案的情况,或受试者参加试验可能影响试验结果或自身安全。
随机访视附加排除标准:
1)随机访视FEV1占预测值<45%或>85%;
2)随机访视FEV1值与筛选访视FEV1值差异>=20%;
3)受试者在导入期依从性差(包括导入期用药依从性<75%或>125%)。
研究中心
| 序号 | 机构名称 | 省 | 市(区) | 地址 | 状态 |
| 1 | 中南大学湘雅三医院 | 湖南省 | 长沙市 | 长沙市河西桐梓坡路138号 | 已启动 |
| 2 | 深圳市宝安区中心医院 | 广东省 | 深圳市 | 深圳市宝安区西乡街道广深公路西乡段233号 | 已启动 |
| 3 | 华中科技大学同济医学院附属协和医院 | 湖北省 | 武汉市 | 武汉市解放大道1277号 | 已启动 |
| 4 | 北京清华长庚医院 | 北京市 | 昌平区 | 北京市昌平区立汤路168号 | 已启动 |
| 5 | 首都医科大学附属北京潞河医院 | 北京市 | 通州区 | 北京市通州区新华南路82号 | 已启动 |
| 6 | 首都医科大学附属北京朝阳医院 | 北京市 | 朝阳区 | 北京朝阳区工人体育场南路8号 石景山区京原路5号 | 已启动 |
| 7 | 北京大学首钢医院 | 北京市 | 石景山区 | 北京市石景山区晋元庄路9号 | 已启动 |
| 8 | 首都医科大学宣武医院 | 北京市 | 西城区 | 北京市西城区长椿街45号 | 已启动 |
| 9 | 东南大学附属中大医院 | 江苏省 | 南京市 | 江苏省南京市鼓楼区丁家桥87号 | 已启动 |
| 10 | 徐州医科大学附属医院 | 江苏省 | 徐州市 | 徐州市泉山区淮海西路99号 | 已启动 |
| 11 | 无锡人民医院 | 江苏省 | 无锡市 | 无锡市梁溪区清扬路299号 | 已启动 |
| 12 | 成都市第七人民医院 | 四川省 | 成都市 | 成都市武侯区致民路十二中街1号 | 已启动 |
| 13 | 成都市郫都区人民医院 | 四川省 | 成都市 | 四川省成都市郫都区德源北路二段666号 | 已启动 |
| 14 | 江西省人民医院 | 江西省 | 南昌市 | 江西省南昌市爱国路152号 | 已启动 |
| 15 | 安徽医科大学附属第二医院 | 安徽省 | 合肥市 | 合肥市经济技术开发区芙蓉路678号 | 已启动 |
| 16 | 安徽省立医院 | 安徽省 | 合肥市 | 安徽省合肥市庐江路9号 | 已启动 |
| 17 | 银川市第一人民医院 | 宁夏回族自治区 | 银川市 | 银川市兴庆区利群西街2号 | 已启动 |
| 18 | 石家庄市人民医院(方北路院区) | 河北省 | 石家庄市 | 石家庄市长安区方北路9号 | 已启动 |
| 19 | 河北中石油中心医院 | 河北省 | 廊坊市 | 廊坊市广阳区新开路51号 | 已启动 |
| 20 | 山西白求恩医院(山西医学科学院) | 山西省 | 太原市 | 太原市小店区龙城大街99号 | 已启动 |
| 21 | 海南省人民医院 | 海南省 | 海口市 | 海口市秀英区秀华路19号 | 已启动 |
| 22 | 西安交通大学第二附属医院 | 山西省 | 西安市 | 西安市西五路157号 | 已启动 |
| 23 | 新疆医科大学第一附属医院 | 新疆维吾尔自治区 | 乌鲁木齐市 | 新疆乌鲁木齐市鲤鱼山路1号 | 已启动 |
| 24 | 遵义医学院附属医院 | 贵州省 | 遵义 | 遵义市汇川区大连路149号 | 已启动 |
| 25 | 贵州医科大学附属医院 | 贵州省 | 贵阳市 | 贵阳市云岩区北京路16号 | 已启动 |
| 26 | 甘肃省人民医院 | 甘肃省 | 兰州市 | 兰州市城关区东岗西路204号 | 已启动 |
| 27 | 吉林大学第二医院 | 吉林省 | 长春市 | 长春市南关区自强街218号 | 已启动 |
| 28 | 吉林省人民医院 | 吉林省 | 长春市 | 长春市工农大路1183号 | 已启动 |
| 29 | 赤峰学院附属医院 | 内蒙古自治区 | 赤峰市 | 赤峰市松山区新城王府大街42号 | 已启动 |