小细胞肺癌免疫治疗的效果怎么样
前言
同为肺癌,相比于非小细胞肺癌而言,小细胞肺癌不仅恶性程度高,而且也缺乏有效的治疗手段,广泛期小细胞肺癌患者的中位生存时间往往不超过1年。即便是对于当前热门的免疫治疗,相比于非小细胞肺癌而言,其疗效也似乎如同鸡肋,其总生存时间相比于化疗而言仅改善2-3个月左右,显然无法与免疫治疗在非小细胞肺癌中的动辄半年以上相媲美。但是,从客观的角度来讲,免疫治疗在小细胞肺癌中还是有其应用价值,只是需要我们从长远角度来看以及注重人群的选择而已。
基于此,在下文中,我们将从循证医学的角度对免疫治疗在小细胞肺癌中的临床应用进行分析,希望能够对大家提供一定的帮助。
免疫治疗在小细胞肺癌中的疗效
尽管免疫治疗早在2018年就拿到了小细胞肺癌三线治疗的适应症(后来因为疗效有限被自行撤回),但是其总体发展进度仍然缓慢。尽管如此,随着几大代表性的临床研究比如IMpower133,CASPIAN ,ASTRUM005以及CAPSTONE-1数据陆续公布出来,免疫治疗联合化疗已经成为了广泛期小细胞肺癌的一线标准治疗模式。尽管各大研究入组的人群不一样,研究所使用的药物也不一样,但是总体的数据都显示相比于EP方案而言,免疫治疗联合化疗的ORR以及PFS改善不明显,OS也仅改善2-3个月。其原因很可能在于小细胞肺癌中PD-L1的表达水平较低,免疫抑制细胞比如Treg的比例较高,而免疫活化的细胞比如CTL比例较低,所以这也能从机制上解释为什么免疫治疗在小细胞肺癌中疗效不佳的原因。
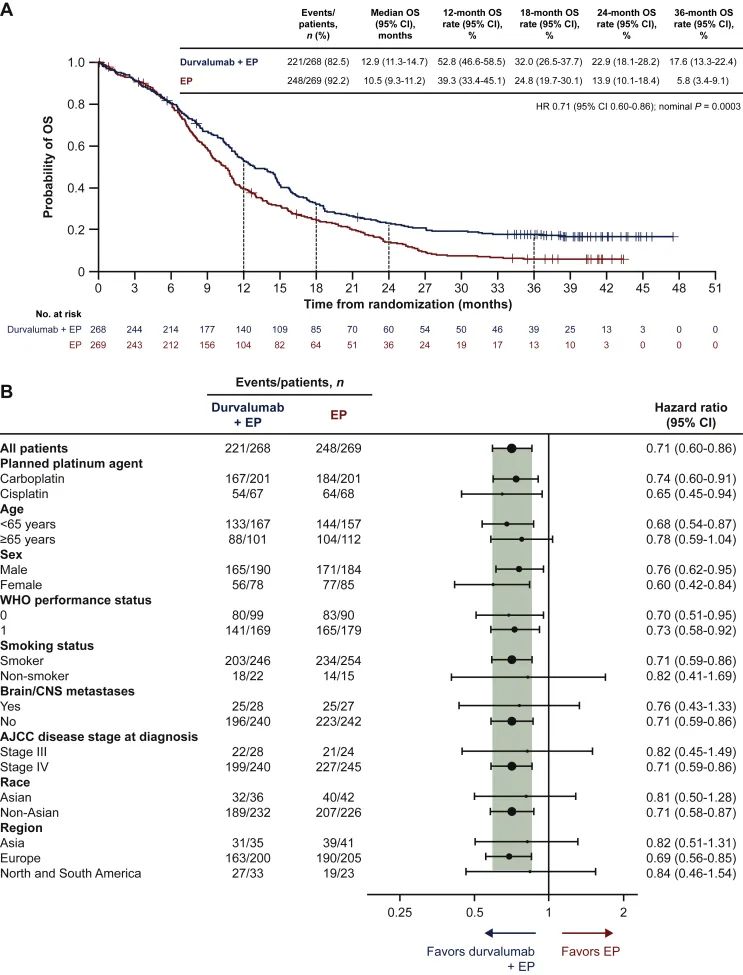
尽管总体OS改善并不明显,但是仅从OS的数值来评估免疫治疗在小细胞肺癌中的治疗价值显然有失偏驳。尤其是在目前越来越多的证据显示,1年、2年的PFS率以及OS率开始逐步取代单纯PFS以及OS数值成为公认的评估免疫治疗长期疗效的主要指标。所以从PFS率以OS率的改善幅度来看,将PD-1联合免疫治疗用于广泛期小细胞肺癌的的一线治疗还是有证据支持的。比如免疫治疗在广泛期小细胞肺癌中的代表性临床研究CASPIAN的长期随访数据就表明,度伐利尤单抗联合EP方案给广泛期小细胞肺癌患者带来的1年,2年以及3年的OS率分别为52.8%、22.9%、17.6%,而仅接受EP方案化疗患者的1年,2年以及3年的OS率分别为39.3%、13.9%、5.8%。这也清楚的表明,免疫治疗确实能够为一部分广泛期小细胞肺癌患者带来长期生存获益,同时也肯定了免疫治疗在小细胞肺癌中的治疗价值。
优势人群的选择
尽管免疫治疗联合化疗确实能够从一定程度上改善小细胞肺癌患者的长期疗效,但是其比例并不高,最终也可能只有不到20%,所以对于临床治疗而言,将这部分潜在的获益人群筛选出来也就是治疗的重点与难点。
尽管目前在小细胞肺癌中还无公认的预测免疫治疗疗效的标记物,但是从接受免疫治疗的小细胞肺癌患者的长期随访数据中还是可以找到一些蛛丝马迹。比如在CASPIAN的临床研究中,尽管最初入组了500多例患者接受度伐利尤单抗联合化疗或者度伐利尤单抗联合替西木单抗(CTLA-4抑制剂),但是最后只有46名患者进入了长期随访。这部分患者其实就是我们一直在找的优势人群,通过仔细分析这些患者的临床特征就会发现,这些患者大都年轻(平均年龄在60岁左右),体能评分状况较好(大都在0-1分),脑转移,肝转移比例较低,同时这些患者大都疗效较好(有效率甚至达到了90%),2年的PFS率在80%以上。
另外,从免疫治疗用于小细胞肺癌临床研究的PFS以及OS的曲线分布特征也可以看出,在免疫治疗的6个月之后,两条曲线(免疫治疗联合化疗 vs 化疗)开始明显分开,这实际上表明,6个月的治疗持续时间很可能是出现疗效差异的一个重要的临界点。简而言之,如果患者在6个月起效的话,其疗效很可能比6个月之后起效患者的疗效要好。此外,6个月以内肿瘤缩小的幅度越大,就越有可能从免疫治疗中得到长期的生存获益。所以,尽管从基因检测的层面无法筛选接受免疫治疗的优势人群,但是通过严格的人群筛选以及细致的临床观察比如肿瘤缩小的幅度,起效时间的快慢以及症状改善等还是非常有可能就在较短的时间内比如6个月以内发现小细胞肺癌接受免疫治疗的优势人群的。
免疫治疗的毒副反应
既然免疫治疗在小细胞肺癌中的长期疗效已经证实,那么除了疗效以外,临床关注的另外一个问题其实就是毒副反应的问题了。几大代表性的临床研究的结果都表明免疫治疗联合化疗用于广泛期小细胞肺癌的毒副反应主要为化疗相关的骨髓抑制以及消化道反应,而免疫治疗相关的毒副反应主要为皮肤反应,内分泌毒性,肝炎,肠炎,肾炎等,3度以上发生率不超过30%, 表明免疫治疗联合化疗用于广泛期肺癌患者的毒副反应不会增加,同时也不会影响患者对治疗的耐受性。
另外,随着近几年对免疫治疗毒副反应认识的加深,越来越多的证据显示免疫相关性毒副反应比如皮肤反应,甲亢,甲减等同免疫治疗的疗效正相关,所以有时候出现免疫相关性毒副反应也许并非坏事,相反这有可能是疗效较好的一种表现,甚至可以用来提前预测疗效。
总结
几大代表性的临床研究数据都显示,免疫治疗能够为一部分广泛期肺癌患者带来长期的生存获益,而且其应用范围还有望进一步扩大,从而为更多患者带来信心与希望。
但是免疫治疗用于小细胞肺癌在当前还存在诸多问题,比如优势人群的筛查,耐药机制的阐明,联合治疗模式的优化比如联合放疗,特殊人群的治疗比如肝脏转移,脑转移等,只有这些问题得到解决,免疫治疗在小细胞肺癌中的应用前景才能进一步扩大,才能为更多患者带来生存获益。
参考文献
1. Horn L, Mansfield AS, Szczęsna A, et al. First-Line Atezolizumab plus Chemotherapy in Extensive-Stage Small-Cell Lung Cancer. The New England journal of medicine. Dec 6 2018;379(23):2220-2229. doi:10.1056/NEJMoa1809064
2. Cheng Y, Han L, Wu L, et al. Effect of First-Line Serplulimab vs Placebo Added to Chemotherapy on Survival in Patients With Extensive-Stage Small Cell Lung Cancer: The ASTRUM-005 Randomized Clinical Trial. Jama. Sep 27 2022;328(12):1223-1232. doi:10.1001/jama.2022.16464
3. Wang J, Zhou C, Yao W, et al. Adebrelimab or placebo plus carboplatin and etoposide as first-line treatment for extensive-stage small-cell lung cancer (CAPSTONE-1): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial. The Lancet Oncology. Jun 2022;23(6):739-747. doi:10.1016/s1470-2045(22)00224-8
4. Paz-Ares L, Chen Y, Reinmuth N, et al. Durvalumab, with or without tremelimumab, plus platinum-etoposide in first-line treatment of extensive-stage small-cell lung cancer: 3-year overall survival update from CASPIAN. ESMO open. Apr 2022;7(2):100408. doi:10.1016/j.esmoop.2022.100408
5. Singh H, Beaver JA, Pazdur R. Immunotherapy for Patients With Small-Cell Lung Cancer-2 Gains, 2 Losses. JAMA oncology. Jan 1 2022;8(1):37-38. doi:10.1001/jamaoncol.2021.4956
6. Paz-Ares L, Dvorkin M, Chen Y, et al. Durvalumab plus platinum-etoposide versus platinum-etoposide in first-line treatment of extensive-stage small-cell lung cancer (CASPIAN): a randomised, controlled, open-label, phase 3 trial. Lancet (London, England). Nov 23 2019;394(10212):1929-1939. doi:10.1016/s0140-6736(19)32222-6
作者:湖北省肿瘤医院黎小兵博士
内容来源:癌之说